甲酰胺
| 甲酰胺 | |||
|---|---|---|---|
| |||
IUPAC名 Methanamide | |||
| 识别 | |||
CAS号 |
75-12-7 |
||
PubChem |
713 |
||
ChemSpider |
693 |
||
SMILES |
|
||
InChI |
|
||
InChIKey |
ZHNUHDYFZUAESO-UHFFFAOYAQ |
||
ChEBI |
48431 |
||
KEGG |
C00488 |
||
IUPHAR配体 |
4739 |
||
| 性质 | |||
化学式 |
HCONH2 |
||
摩尔质量 |
45.04 g·mol⁻¹ |
||
密度 |
1.133 |
||
熔点 |
2-3 °C |
||
沸点 |
210 °C |
||
蒸氣壓 |
0.08 mmHg @20 °C |
||
pKa |
23.5 (DMSO)[1] |
||
| 危险性 | |||
闪点 |
154 °C (闭杯) |
||
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |||
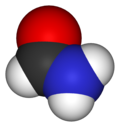
甲酰胺是甲酸衍生出的酰胺,分子式为HCONH2。它是无色液体,与水混溶,有与氨类似的气味。主要用于生产磺胺类药物,合成维生素及用作纸张和纤维的软化剂。纯的甲酰胺可以溶解许多不溶于水的离子化合物,因此也被用作溶剂。
目录
1 用途
2 生产
3 参见
4 参考资料
用途
- 甲酰胺是玻璃化冷冻液的组分之一,被用于超低温保存组织和器官。
- 甲酰胺被用作凝胶电泳中RNA的稳定剂,也用于稳定毛细管电泳中的变性单股DNA。
烧结时可在溶胶凝胶中加入甲酰胺以防止开裂。- 纯的甲酰胺可用作纳米薄膜聚合物静电自组装中的替代溶剂。[2]
生产
实验室和过去的工业上,都先以甲酸和氨反应生成甲酸铵,再使其热分解来制备甲酰胺:
HCOOH + NH3 → HCOONH4
- HCOONH4 → HCONH2 + H2O
现在工业上以甲酸甲酯的氨解反应来制取甲酰胺:
- HCOOCH3 + NH3 → HCONH2 + CH3OH
参见
N,N-二甲基甲酰胺
参考资料
^ F. G. Bordwell, J. E. Bartmess and J. A. Hautala. Alkyl effects on equilibrium acidities of carbon acids in protic and dipolar aprotic media and the gas phase. J. Org. Chem. 1978, 43 (16): 3095–3101. doi:10.1021/jo00410a001.
^ Vimal K. Kamineni, Yuri M. Lvov, and Tabbetha A. Dobbins. Layer-by-Layer Nanoassembly of Polyelectrolytes Using Formamide as the Working Medium. Langmuir. 2007, 23 (14): 7423–7427. doi:10.1021/la700465n.
|


Comments
Post a Comment