钾
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外觀 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
金属:银白色  钾的光谱线 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 概況 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名稱·符號·序數 | 钾(Potassium)·K·19 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 元素類別 | 碱金属 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
族·週期·區 | 1 ·4·s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 標準原子質量 | 39.0983(1) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子排布 | [氩] 4s1 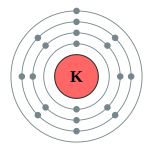 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 歷史 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 發現 | 汉弗里·戴维(1807年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分離 | 汉弗里·戴维(1807年) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理性質 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物態 | 固体 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度 | (接近室温) 0.862 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
熔點時液體密度 | 0.828 g·cm−3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔點 | 336.53 K,63.38 °C,146.08 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 沸點 | 1032 K,759 °C,1398 °F | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 三相點 | 336.35 K(63 °C), kPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熔化熱 | 2.33 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 汽化熱 | 76.9 kJ·mol−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 比熱容 | 29.6 J·mol−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
蒸汽壓 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子性質 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 氧化態 | +1 (强碱性) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電負性 | 0.82(鲍林标度) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電離能 | 第一:418.8 kJ·mol−1 (更多) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子半徑 | 227 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共價半徑 | 203±12 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 范德華半徑 | 275 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 雜項 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 晶體結構 | 体心立方 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁序 | 顺磁性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電阻率 | (20 °C)72 n Ω·m | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 熱導率 | 102.5 W·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 膨脹係數 | (25 °C)83.3 µm·m−1·K−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
聲速(細棒) | (20 °C)2000 m·s−1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 楊氏模量 | 3.53 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 剪切模量 | 1.3 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 體積模量 | 3.1 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 莫氏硬度 | 0.4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 布氏硬度 | 0.363 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS號 | 7440-09-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 最穩定同位素 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
主条目:钾的同位素
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
钾(拉丁語:Kalium,化学符号:K[1])是原子序数为19的化学元素,银白色有光泽的1A族碱金属元素,质软,和鈉的化學性質相似但更活泼。
目录
1 性質
2 发现
3 名称由来
4 分布
5 制备
6 同位素
7 應用
8 对人体的影响
8.1 營養代謝
8.1.1 低血鉀(Hypokalemia)
8.1.2 高血鉀(Hyperkalemia)
8.1.3 相關遺傳性疾病
9 参考资料
性質
钾的熔点、硬度低,比钠更活泼,在空气中很快氧化。钾的密度小于水,大于煤油。鉀和水會產生劇烈反應(產生高温使自己熔成一個銀白色的球,釋放大量氫,使金属球在水面高速移動,氢气燃烧,可以看到紫藍色的火焰,生成氢氧化钾。方程式如下:
- 2K+2H2O====2KOH+H2↑{displaystyle {rm {2K+2H_{2}O{=!=!=!=}2KOH+H_{2}uparrow }}}
钾可以和卤族、氧族元素反应,还可以使其他金属的盐类还原(熔融状态下),对有机物有很强的还原作用。
鉀容易與氧反應 在表面形成紫色的氧化鉀
- 4K+O2====2K2O{displaystyle {rm {4K+O_{2}{=!=!=!=}2K_{2}O}}}
鉀為爆炸性和易燃的物質,一般以汽油或煤油封存。
发现
1807年由英国化学家戴维首次用电解法从熔融氢氧化钾中制得金属钾,并定名。
名称由来
拉丁語:kalium,這個單字不存在於古典拉丁語中,這是由永斯·贝采利乌斯創造的新拉丁文名詞。這個名詞起源於阿拉伯语:القَلْيَه(al-qalyah),本義為植物灰燼。qaly是刺沙蓬一类的植物,古人焚烧这种植物,从灰烬中可以的得到不纯的钾盐和钠盐混合物,进而和石灰水反应可以得到强碱溶液。這個阿拉伯名詞傳入歐洲後,被拼為alkali,意為鹼。永斯·贝采利乌斯以此命名钾为kalium。
鉀英文名「potassium」則由「Potash」衍生而來。当时的人们焚烧木材,其灰烬用水浸泡,取上清液,在铜锅里煮沸除去水分,可得不纯的钾盐混合物,称为Potash(Pot-Ashes:pot锅,ash灰烬)。戴维使用的氢氧化钾就是从Potash转化而来的,因此将钾命名为potassium。
分布
钾在自然界中只以化合物形式存在。在云母、钾长石等硅酸盐中都富含钾。钾在地壳中的含量约为2.09%,居第七位。在海水中以钾离子的形式存在,含量约为0.1%。钾在海水中含量比钠离子少的原因是由于被土壤和植物吸收多。在动植物体内也含有钾。正常人体内约含钾175克,其中98%的钾贮存于细胞液内,是细胞内最主要的阳离子。
制备
这种元素通过将其常见的氢氧化物进行电解而得到。將氢氧化钾与卤化物进行熔融电解,再经真空蒸餾製得。
早期,由法国化学家給呂薩克和泰纳尔发明的隔绝空气加强热于碳酸钾、碳粉、铁粉、明矾混合物的方法也被用于制备粗钾,并被用于当时的一种打火机中。
同位素
已发现的钾的同位素共有16种,包括钾35至钾50,其中只有钾39和钾41是稳定的,其他同位素都带有放射性。
應用
钾主要用作还原剂及用于合成中。钾的化合物在工业上用途很广。钾盐可以用于制造化肥及肥皂。钾对动植物的生长和发育起很大作用,是植物生长的三大营养元素之一。
鉀金屬在工業上可作為較強的還原劑。鈉鉀合金在一些特殊冷卻設備中作為熱傳導的媒介。
对人体的影响
營養代謝
鉀是人體必需的礦物質營養素,是體細胞內主要的陽離子,體重70公斤的成年男性體內,鉀含量約3500mEq。飲食中的鉀離子在小腸中很容易被吸收。人體鉀離子主要流失途徑有80-90%是由腎臟經尿液排除,其餘10-20%是由糞便排出。腎臟對於鉀離子具有調控作用,藉以維持鉀離子濃度在正常範圍內。基於彌補身體的流失量以維持正常儲存及血漿濃度的平衡,成人每日的最小需要量為200 mg。含鉀豐富的食物包括乳制品、水果、蔬菜、瘦肉、内脏、香蕉、葡萄干等。飲食建議攝取量如下:
| 年齡 | 鉀充足攝取量 (公克/天) |
| 嬰兒0-6個月 | 0.4 |
| 嬰兒7-12個月 | 0.7 |
| 兒童1-3歲 | 3.0 |
| 兒童4-8歲 | 3.8 |
| 9-13歲 | 4.5 |
| 14歲以上 | 4.7 |
| 孕婦 | 4.7 |
| 哺乳婦 | 5.1 |
钾可以调节细胞内适宜的渗透压和体液的酸碱平衡,参與细胞内糖和蛋白质的代谢。有助于维持神经健康、心跳规律正常,可以预防中风,并协助肌肉正常收缩。在摄入高钠而导致高血压时,钾具有降血压作用。細胞對鉀的調節與鈉鉀泵(Na+/K+ pump)和鉀離子通道有關。
低血鉀(Hypokalemia)
人体钾缺乏可引起心跳不规律和加速、心电图异常、肌肉衰弱和烦躁,最后导致心跳停止。一般而言,身体健康的人,会自动将多余的钾排出体外。但肾病患者则要特别留意,避免摄取过量的钾。
導致低血鉀的原因包括:長期嘔吐、腹瀉、糖尿病酸中毒、神經性厭食症、長期營養不良、慢性酒精中毒、腎上腺腫瘤、燙傷、臨床上常見的電解質異常、吸收不良或血鉀過度流失、或使用某些藥物而使血中之鉀濃度不夠。輕度低血鉀(血清鉀濃度3.0-3.5meq/L)經常是沒有症狀;中度低血鉀(血清鉀濃度2.5-3.0meq/L)有非特異性的症狀像是虛弱、疲倦、便秘等;嚴重低血鉀(血清鉀濃度<2.5meq/L)可能發生肌肉壞死,甚至呼吸肌麻痺衰竭。補充鉀離子是治療低血鉀的最根本辦法。[3][4]
高血鉀(Hyperkalemia)
血中鉀離子濃度高於5.5 mEq/L時稱為高血鉀,可能因攝取過多、排泄減少、或因鉀離子由細胞內轉移至細胞外液等原因造成。一般以腎臟衰竭病患容易發生高血鉀。當人體發生高血鉀時,會有血壓降低、心律不整、心電圖改變、嚴重時會有心室纖維顫動、心跳停止。神經肌肉的症狀在早期為肌肉震顫、痙攣、感覺異常等情形,晚期則會有肌肉無力、弛緩性麻痺、呼吸停止。此外也會出現噁心、嘔吐、腸蠕動增加、腹瀉、腹絞痛等消化系統的症狀及少尿、無尿等泌尿系統的症狀。[5]
相關遺傳性疾病
家族性低血鉀週期性無力症(familial hypokalemic periodic paralysis),為自體顯性遺傳疾病,相當罕見。突變的基因CACNL1A3是一種鈣離子通道。疾病的特徵是突然發生的肌肉麻痺與血清鉀濃度<2.5meq/L。血鉀減少的原因可能是大量攝取碳水化合物或鈉離子而誘發,會在24小時內自然消退,但有時會引起致命性心率不整[6]。
李德爾氏綜合徵(Liddle's syndrome)為隱性遺傳疾病。此遺傳異常會因為礦物皮質醛酮增高,影響到腎臟離子輸送活性,刺激集尿管細胞對鈉離子的再吸收,造成代謝性鹼中毒和低血鉀。
巴特氏症候群(Bartter's syndrome)為亨利氏環(loop of Henle)和近曲小管的鈉運輸蛋白(chloride-associated sodium transporters)失去活性或功能[7]。
吉特曼氏綜合症(Gitelman's syndrome)是腎脏遠曲小管(distal convoluted tubule)鈉運輸蛋白失去活性或功能。
参考资料
^ 夏征农、陈至立 (编). 《辞海》第六版彩图本. 上海: 上海辞书出版社. 2009年: 第3227页. ISBN 9787532628599.
^ Institute of Medicine(2005)Dietary Reference Intakes for Water, Potassium, Sodium, Chloride, and Sulfate. pp. 186-268. National Academy Press, ISBN 978-0-309-53049-1
^ http://www.cgb.com.tw/j2j0/cus/cus1/hel/hel4/40003.jsp
^ 存档副本. [2007-12-22]. (原始内容存档于2007-11-04).
^ http://www.cgb.com.tw/j2j0/cus/cus1/hel/hel4/40003.jsp
^ [1]
^ [2][永久失效連結]
元素周期表(碱金属) | ||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| | IA 1 | IIA 2 | IIIB 3 | IVB 4 | VB 5 | VIB 6 | VIIB 7 | VIIIB 8 | VIIIB 9 | VIIIB 10 | IB 11 | IIB 12 | IIIA 13 | IVA 14 | VA 15 | VIA 16 | VIIA 17 | VIIIA 18 | ||||||||||||||||||
1 | H | | He | |||||||||||||||||||||||||||||||||
2 | Li | Be | | B | C | N | O | F | Ne | |||||||||||||||||||||||||||
3 | Na | Mg | | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||
4 | K | Ca | | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||
5 | Rb | Sr | | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||
6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | ||||
7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | ||||
| ||||||||||||||||||||||||||||||||||||
| |||||||||||||
|



Comments
Post a Comment