化學
科学 系列条目  | ||||||||
|---|---|---|---|---|---|---|---|---|
| ||||||||
| ||||||||
| ||||||||
| ||||||||
| ||||||||
| ||||||||
| ||||||||
| ||||||||

化学是研究物质组成结构以及属性,和它们在化学反应当中变化的科学

在化学反应当中,连接原子的键断裂并重新形成,形成了具有不同性状的物质。在一个巨热的炼钢炉当中,氧化铁即一种化合物和一氧化碳形成了铁(一种单质)和另外一种化合物:二氧化碳。

1931年的化學實驗室

在科隆大學生物化學學院實驗室中的工作檯
化學是一門研究物質的性質、組成、結構、以及变化规律的基礎自然科學。化學研究的對象涉及物質之間的相互關係,或物質和能量之間的關聯。傳統的化學常常都是關於兩種物質接觸、變化,即化學反應[1],又或者是一種物質變成另一種物質的過程。這些變化有時會需要使用電磁波,當中電磁波負責激發化學作用。不過有時化學都不一定要關於物質之間的反應。光譜學研究物質與光之間的關係,而這些關係並不涉及化學反應。准确的说,化学的研究范围是包括分子、离子、原子、原子团在内的核-电子体系。[2]
「化學」一詞,若單從字面解釋就是「變化的學問」之意。化学主要研究的是化学物质[3]互相作用的科学。化學如同物理皆為自然科學之基礎科學。很多人稱化學為「中心科學」,因為化學為部分科學學門的核心,連接物理概念及其他科學,如材料科學、纳米技术、生物化學等。
研究化學的學者稱為化學家。在化學家的概念中一切物質都是由原子或比原子更細小的物質組成,如電子、中子和質子。[4]但化学反应都是以原子或原子团为最小结构进行的。若干原子通过某种方式结合起来可构成更复杂的结构,例如分子、離子或者晶體。
當代的化學已發展出許多不同的學門,通常每一位化學家只專精於其中一、兩門。在中學課程中的化學,化學家稱為普通化學(德語:Allgemeine Chemie,英语:General Chemistry,法语:Chimie Générale)。普通化學是化學的導論。普通化學課程提供初學者入門簡單的概念,相較於專業學門領域而言,並不甚深入和精確,但普通化學提供化學家直觀、圖像化的思維方式。即使是專業化學家,仍用這些簡單概念來解釋和思考一些複雜的知識。
目录
1 詞源
2 歷史
2.1 人类早期对火的认识
2.2 炼金术
2.3 早期化学
2.4 现代化学
3 當代化學
4 基本概念
4.1 原子
4.2 元素
4.3 物质
4.3.1 命名法
4.4 分子
4.5 離子和盐
4.6 酸碱性
4.7 氧化还原
4.8 化學品
4.9 化合物
4.10 摩尔以及物质的量
4.11 化學鍵
4.12 分子间力
4.13 物理特性
4.14 化學反應
4.15 平衡
4.16 能量
4.17 化学定律
4.18 化学工业
5 学科分类
6 参見
7 註釋及参考資料
7.1 参考文獻
8 外部連結
詞源
英語中的「化學」(chemistry)一字的語源有多种说法。一种说法认为是由「鍊金術」(alchemy)得名的。英語中「alchemy」一词源於古法語的「alkemie」和阿拉伯語的「al-kimia」,意為「形态变化的学问」(the art of transformation)。阿拉伯语中的「kimia」一字則源於希腊語。亦有另一种说法认为英語中的「chemistry」一字源自埃及语中的「kēme」,意思是「土」(earth)。
在中國,「化学」一词最早出现在1857年墨海书馆出版的期刊《六合叢談》[5]。伟烈亚力提及王韬在其日记中记载了从戴德生处听闻的「化学」一词[6][7]。一般認為中文中的“化学”一词是徐寿翻译英国人的书《化学鉴原》一书时发明的。
「化学」一词被介绍到日本,取代了原先日语中的译法「舍密」[8][5]。
歷史
人类早期对火的认识
最早的化學要算是人類對火的研究。對於當時的人來說,火可以將一種物體變成另一種物體,所以成為了當時人最有興趣研究的現象。如果沒有火,人類不會發現到鐵和玻璃的製造方法。
炼金术
人類發現了黃金這種貴重的金屬之後,很多人轉移研究怎樣把其他物質變成黃金。公元前300年至1500年,煉金術士皆研究如何將一些便宜的金屬轉化成黃金,因此累積了金屬的提取和處理有關的觀察和技術。有些煉金術士主要的工作是製造藥物,中國當時亦有所謂煉丹術。2000年前,人類已廣泛使用金、銀、汞、銅、鐵和青銅。當時的人類文明,對於陶瓷、染色、釀造、造紙、火藥等在工藝方面已有一定成就,在技術經驗上,對物質變化的理解已有一定觀察和文獻累積。
早期化学

门捷列夫像
早期化學家收集了很多不同物質的資料。在17世紀以前,化學成就並不大(燃素說、煉金術),其中較有成就者如羅伯特·波義耳。到了1750年,化學仍帶有神秘色彩,並為不正確的理論支配著。直到1773年,安托万-洛朗·德·拉瓦锡提出了質量守恆定律,並以氧化還原反應解釋燃燒現象,推翻了盛行於中世紀的燃素說,才開啟了現代化學之路;他因此被尊崇為「化學之父」。接著道尔顿整合當時的化學知識,並以自身的實驗所得提出了劃時代的原子說。此後,一些化學家相繼發現了各種化學元素,後來門得列夫建立了元素週期表令化學視界更臻完備。1901年,化學家諾貝爾以其遺產成立了諾貝爾化學獎,以表揚在化學領域對人類有貢獻者。
现代化学
现代化學始於20世紀初期蓬勃發展的量子力學。萊納斯·鮑林引進量子力學解釋化學鍵的本質,得以用波函數的線性疊加來描述。質子、中子和電子的發現,使化學真正由原子尺度來理解化學反應。量子力學和電子學的發展,使得許多新型儀器得以開發,來探索和分析化合物的結構和成分,如光譜儀、色谱仪、核磁共振仪和質譜儀等。
當代化學

正在做實驗的人
當代化學大致分為四大學門,各學門又有許多延伸的子學門和應用化學領域。
四大學門主要為:
物理化學是從物理角度分析化學原理的化學學門,可謂近代化學的原理根基。物理化學家關注於分子如何形成結構、動態變化、分子光譜的根本原理,以及平衡態等基本問題,涉及熱力學、量子力學、統計力學等重要物理領域。大體而言,物理化學為四大學門中最講求數值精確以及理論架構嚴謹的學門。
分析化學開發分析物質成分、結構与量的方法,使化學物质成分得以定性或定量,化學物质結構得以確定。从分析手段分,分析化学又可分为化学分析和仪器分析。分析化學是化學家最基礎的訓練之一。化學家在實驗技術和基礎知識上的訓練,皆得力於分析化學。當代分析化學著重儀器分析,常用的仪器分析手段有如下几种:光谱法(例如紫外分光光度法、红外光谱法、原子发射光谱法、原子吸收光谱法、X射线衍射法、拉曼光谱法等)、色谱法(例如薄层色谱法、气相色谱法、液相色谱法、电泳法等)、电化学分析(例如伏安法、电致发光法、电导分析法等)、质谱法、能谱法等。
有機化學研究碳、氫、氧、氮、硫等元素組成的化合物的化學學門。有機化學主要研究有機化合物的合成途徑和方法、機構和物理性質。由於有機化學高度的應用性和悠久的發展歷史,通常被普羅大眾視為當代化學的代名詞。有機合成和新反應途徑的開發,對於藥物,天然物,生物和材料高分子的開發,都是極為重要的一環,對於化學工業有極大的影響。
無機化學有機化合物以外元素的化學領域,研究化合物的合成途徑和方法,機構和物理性質,最常見的分子體系為金屬化合物。有機和無機化學領域常有交疊,甚至有密不可分的趨勢。有機金屬化學就是一門結合有機和無機領域的化學。
其他延展和應用的學門:

移液器,一種生化常用的實驗儀器
理論化學從物理的理論去解釋各種化學現象的學門。
計算化學由於分子體系的複雜性,分子的反應,動態,結構,經常是無法完全以量子力學做計算的。因此計算化學提供各種簡約的計算方法,來預測並輔助實驗結果的推斷。實用性上已有諾貝爾獎的肯定,如1998年獲諾貝爾化學獎的密度泛函方法。
生物化學是研究生物體內發生的化學反應和相互作用的學科,被應用於研究細胞中各組分(例如:蛋白質,碳水化合物,脂類,核酸以及其他生物分子)的結構和功能。生物化學被廣泛應用於蛋白質各項化學性質的研究,特別是應用於酶促反應的研究。
熱化學是以热力学的观点来研究化学,以焓、熵等状态函数来描述和预言化学物质稳定性和化学反应发生的结果。
電化學是研究各種因為電推動而發生的化學作用或者會在運作途中産生電力的化學作用的科學學門。生活中常見的各種電池就是電化學的研究成果。
光化學研究各種化學物質,受到各種頻率光線照射之後的化學反應變化。
藥物化學研究化學物質怎樣用於藥劑中,從而改變藥劑的功效,做出醫療的作用。它其實是幾個化學門派,包括有機化學、無機化學、生物化學、物理化學,及幾個不屬於化學的科學學門,包括:藥劑學、分子生物學和統計學的結合。
量子化學用量子力學及其他純理論手段解釋各種化學現象。
核子化學研究不同的次原子粒子怎樣走在一起,形成一個原子核,及研究一個原子核中的物質如何變化。
放射化學是化學的一個分支,旨在研究那些參與化學反應的物質屬於或帶有放射性同位素的化學反應的一門學科。例如:採用碘的放射性同位素125I標記各種蛋白質或激素,以便利用放射免疫分析技術,檢測血清標本之中相應物質的浓度。
天体化學研究外太空的化學物質,分析它們的成分、結構與地球上的物質有什麼不同。
大氣化學是一種對地球大氣層及其他星球的大氣層的研究。大氣化學都會研究環境變化途中發生過什麼化學反應,是大氣科學的一個重要分支學科。
環境化學研究化學物質進入不同自然環境,經物理、化學、生物反應後,形成的產物是否對人體及生態造成危害。
綠色化學研究怎樣從化學角度減低污染。
資訊化學用電腦去解決化學上的問題。
地球化學研究地殼中各種物質的化學特性,解釋它們的構造。
石油化學從化學角度研究石油及天然氣的特性及煉油技術。
高分子化學研究比較大的分子,即是高分子,例如發泡膠怎樣造出來和有些什麼特性。高分子化學亦會研究怎樣令很多分子結合為一粒高分子。
超分子化學研究共價鍵以外各種化學鍵,例如:氫鍵、范德華力、疏水效應的運作。
基本概念
原子
一粒原子是由原子核及外圍帶負電荷的電子(称为核外电子)組成的粒子,一般而言是化學研究的最小尺度範疇。原子核通常是由質子和中子組成。与通常的物理概念不同的是,单一的质子在化学领域被认为是1H(氕)原子核,也就是说原子核内必然含有质子,但可能不含中子。
電子帶負電荷,質子帶正電荷,個數相同使得電荷平衡,令整個原子呈电中性。当核外电子数与原子核内质子数不相同时,则形成离子。通常认为离子也是原子的一种。

氦原子的结构示意图
元素
拥有相同质子数的同一类原子被称为“元素”。例如,氫這種元素中所有原子都是只有一粒質子。這個概念換過來說亦可:所有原子核中有六粒質子的原子都是碳,所有原子核中有九十二粒質子的都是鈾。元素亦有另一定義,就是所有不可以用化學方法分解的物質都是元素。
在這麼多種列舉元素的方法中,最常用和最方便的莫過於元素週期表。週期表根據原子序數來排列原子,而原子序數就是一粒原子中質子的數量。因為這個奇怪的排列,排在一起的元素,無論是同一個直行、同一個橫行還是純粹在附近,都有一些大致上固定的關係。
同一種元素可能有很多個不同的核素。它們的质子数相同而中子数不同,因而化学性质相同。但由于它们的中子数不同,造成原子核稳定性不同,而造成某些核素具备放射性。同一种元素的不同核素在元素周期表内占据同一个位置,因此同一种元素的不同核素互称同位素。例如1H(氕)与2H(氘)互称同位素。

元素周期表
物质
化学物质是指一种物体,它既确定了其化学组成,也确定了它的化学性质[9]。严格的来讲,混合的化合物,元素等都不能算是化学物质,只能说是化学药品或者说化学制品。大多数我们日常生活碰到的化学品都是混合物,比如空气、合金、生物制品。
命名法
物质的命名法在化学语言当中是最严格的一环。早在很久以前,化合物的命名是由其发现者自行决定的,这样则导致了命名的困难和混乱。而现在我们最常用的还是国际纯粹与应用化学联合会 (International Union of Pure and Applied Chemistry) (IUPAC)命名方法。它用一个命名系统让所有的化合物都有一个独有的名称和代码。有机化合物通过有机命名[10]系统命名;而无机化合物通过无机命名[11]系统命名。而通过化学索引服务(Chemical Abstracts Service),我们可以轻松的通过CAS号(CAS registry number)来找到每一个化合物的性质、特性、命名和结构。
分子

一个分子结构式描述了化学键以及它在分之中所连接的原子的位置,图上为紫杉醇的分子结构
一個分子是化合物的最基本结构,不用化學方法是拆不開的。大部分分子都是由兩個或以上原子組成,但是都有些特例,例如氦氣分子,只有一個原子。這些原子,如果多於一個,是通过化學鍵結合。
離子和盐
離子是带电荷的物质,可以由原子或分子失去或得到电子形成。正離子(例如鈉離子Na+)和負離子(例如氯離子Cl−)結合可以成為電荷中性的鹽(例如食鹽NaCl)。有些離子是由幾個原子組成,而它們進行化學作用的時候又不會分离,例如磷酸根離子(PO43−)、銨離子(NH4+)。气相的离子通常被称为等离子体。
酸碱性
物质可以被分类为一种酸或者是一种碱。通常我们有几种进行酸碱分类定义的理论。其中最简单的要数阿累尼乌斯理论(Arrhenius theory),它认为:酸是能够在水当中电离出水合氢离子的物质;而相反碱则是在水当中电离出氢氧根离子的物质。而酸碱质子理论(Brønsted–Lowry acid-base theory)则认为酸是能够在化学反应中给其他物质氢离子的物质;而碱则是相应能得到氢离子的物质。第三种理论被称作是路易斯酸碱理论(Lewis acid-base theory),它是基于形成化学键之上的。路易斯理论认为:酸是在键的形成当中接受了一对电子;而碱则是在形成键的过程中给予了其他物质一对电子。因此,一个物质如果对于不同的酸碱理论来说,可能在此是酸,在另外一个理论来说却是碱。
酸性强度的衡量方法主要有两种:第一种是阿累尼乌斯定义的也就是我们最常用的pH,它是通过衡量一个溶液当中氢离子的浓度来确定酸性的大小。它的计算方法是pH=-log10[H+],也就是pH等于氢离子浓度的负对数(以10為底)。因此可以说,拥有更高浓度的氢离子溶液,其pH越低而酸性更强。第二种是Brønsted–Lowry定义,也就是酸解离常数(Ka),它衡量的是物质作为酸的时候给予氢离子的能力。因此一个酸性越强的物质,其Ka更高,更具有给予氢离子的的倾向。同样的我们可以用pOH代替pH, Kb代替Ka来说明碱性强度。
氧化还原
氧化还原的概念和一个物质的原子获取或者给予电子的能力有关。物质拥有氧化其他物质的能力就被成为氧化性,而此物质被成为氧化剂(oxidizing agents),或者成为氧化物。一个氧化剂能够将电子从其他的物质上移走。相应的,具有还原其他物质的物质被称作有还原性而成为还原剂(reducing agents)或者成为还原物。一个还原试剂能够传递给其他物质电子并且氧化自身。而正因为其“给予”了其他物质电子,它还被称为供电子物。氧化还原的性质与氧化数(oxidation number)有关--其实真正的给予或者获取完成的电子并不存在。所以,氧化过程被定义为增加了氧化数,而还原则是降低的氧化数。
化學品
化學品泛指一切有確實化學構造及化學成份的物質,所以又稱化學物質。它們可以是元素、化合物或混合物。日常生活中,我們會遇到的東西多數都是混合物,例如合金。
化合物

一顆氯化鈉(食鹽)的結晶
化合物是一些以不同元素用固定比例結合而成的物質。成份的比例決定了它的化學特性。例如水是用氫同氧以二比一組合而成,组成水分子的三個原子之間构成了104.5度的健角。不同化合物及元素之間的變化稱為化學反應。
摩尔以及物质的量
摩尔(英语:mole,仅台湾地区使用莫耳一词)是物质的量的国际单位,符号为mol。1摩尔是所含基本微粒个数与12克的碳-12(612C{displaystyle {}_{6}^{12}!{mbox{C}}}
一种物质的摩尔质量与分子量,在使用国际单位制时,在数值上相等。
化學鍵
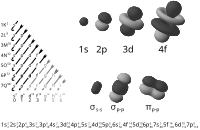
原子电子以及分子轨道
化學鍵是指組成分子或材料的粒子之間互相作用的力量,其中粒子可以是原子、離子或是分子。化學鍵的物理本質來自於粒子和粒子之間的静電力,量子力學上意指原子間電子的波函數線性疊加。化學鍵是化學最重要的概念之一,物理理論本質由萊納斯·鮑林建立。化學家為能簡潔表述化學鍵並規避量子力學的複雜性,將化學鍵分類為共價鍵、離子鍵和金屬鍵,較弱的鍵結如氫鍵及较特殊的配位相互作用等。無論分類為何,其物理本質都是相同的。
分子间力
分子间力是不同分子之间的作用力,主要有氢键,范德华力,亲水作用/疏水作用等,这种作用力比化学键弱,容易打开或重新组合,但是是形成分子空间排列和架构的重要作用力,是现代化学的重要研究方向之一。
物理特性

水湧上沙灘造成浪,就是水與沙的物理特性
物質有時會是液體,有時會是固體,有時會是氣體,這些叫作物質的相態。一件物質是否軟、透不透光、透光的話它的折射率是多少,這些都是一件物質的物理特性。總而言之,物理特性即是一種物質不靠化學作用都可以斷定到的特性。
化學反應

氯化氢同氨发生化學反應生成氯化銨
化學反應,亦称化学变化是一種物質轉變為另一種物質的過程,涉及分子中原子的交換和化學鍵的轉移、形成或消失。化學反應形成的改變既可令很多獨立的分子結合,也可將一個較大型的分子拆開成為很多獨立的小分子,甚至是同一分子內有原子移動,即使原子的數量沒有改變,但仍會構成化學反應。
平衡
雖然平衡概念在科學各領域都得到廣泛的應用,但在化學中,化學平衡是指化學成分中出現多種不同狀態的可能性,例如在可以彼此反應的幾種化合物的混合物中,或當物質可以以多於一種相態存在的時候。
即使有著不變的化學組成,但在平衡系統中的化學物質通常並非處於靜止狀態;這些物質的分子會互相繼續進行反應,從而產生動態平衡。因此,化學平衡描述了諸如化學成分之類的參數隨時間保持不變的狀態。
能量
化学定律
化學反應的守恆必須符合物理守恆定律,反應前後應符合:
質量守恒定律:一個化學反應發生,物質的總質量不會有任何變化。
能量守恒定律:化學反應所產生的能量總和不變,只是能量形式依照反應模式而變化。引出三个重要概念:平衡,热力学,动力学。
電荷守恆定律:化學反應前後的電荷數應守恆。- 阿伏伽德罗定律
- 比尔-朗伯定律
波义耳定律(1662年,压力和体积相关)
查理定律(1787年,体积和温度相关)- 斐克扩散定律
盖吕萨克定律(1809年,壓力与温度相关)- 亨利定律
- 赫士定律
- 定比定律
- 倍比定律
拉乌尔定律:理想溶液在一固定温度下,其内每一组元的蒸气分压与溶液内各该组元的摩尔分数成正比,其比例系数等于各该组元在纯态下的蒸气压。(物理化学的基本定律之一)
化学工业
化学工业(化工)是当代经济活动当中重要的一部分。全球50大化学品制造商在2004年共销售了5870亿美元的业绩,其中利润占据了8.1%,其中研发成本占据了2.1% [12]
学科分类
无机化学是研究无机化合物的化学。
- 元素化学
无机合成化学主要是經由各式各樣的无機反應來建構無機分子。
有机化学是研究有机化合物的结构、性质、制备的学科,又称为碳化合物的化学。
有机金属化学是有机化学和無機化學交疊的一門分支課程,研究含有金屬(包括類金屬)和碳原子鍵結的有机金属化合物,其化學反應、合成等各種問題。- 有机合成化学
- 天然有机化学
分析化学是开发分析物质成分、结构与量的方法,使化学物质成分得以定性或定量,化学物质结构得以确定。
- 按分析目标分,可分为定性分析与定量分析
定性分析主要任务是确定物质的组分
定量分析需要测定物质中各组分的含量的分析方法
- 按分析手段分,可分为化学分析与仪器分析
- 化学分析
仪器分析是用儀器的物理學方法,測量物質的物理和化學性質的参數,並實驗其變化,以此判斷其化學成份,元素含量,甚至化學結構等。
- 按分析目标分,可分为定性分析与定量分析
生物化学是研究生物体中的化学进程的一门学科,常常被简称为生化。
材料化学(材料科学或材料工程)是一个多学科领域,涉及物质的性质及其在各个科学和工程领域的应用。它是研究材料的制备或加工工艺、材料的微观结构与材料宏观性能三者之间的相互关系的科学。
核化学又称为核子化學,研究原子核(稳定性和放射性)的反应、性质、结构、分离、鉴定等的一门学科。
物理化学是一门从物理学角度分析物质体系化学行为的原理、规律和方法的學科,可謂近代化學的原理根基。
理论化学运用非实验的推算来解释或预测化合物的各种现象。近年来,理论化学主要包括量子化学,即应用量子力学来解决化学问题。
量子化学是应用量子力学的规律和方法来研究化学问题的一门学科。
结构化学是研究原子、分子和晶体结构以及结构与性能之间关系的学科。近几十年,这门学科获得迅速发展,结构化学观点不仅渗透到化学各个分支学科领域,同时在生物、材料、矿冶、地质等技术科学中也得到应用
其他还有诸如放射分析化学、同位素化学、辐射化学、核燃料、反应堆和裂变产物化学、地球化学、海洋化学、大气化学、环境化学、宇宙化学、星际化学、药物化学、神经化学、农业化学、石油化学、木材化学、土壤化学、煤化学、食品化学、化学地理学、天体化学、岩石化学、空间化学及胶体与界面化学等
参見
.mw-parser-output .refbegin{font-size:90%;margin-bottom:0.5em}.mw-parser-output .refbegin-hanging-indents>ul{list-style-type:none;margin-left:0}.mw-parser-output .refbegin-hanging-indents>ul>li,.mw-parser-output .refbegin-hanging-indents>dl>dd{margin-left:0;padding-left:3.2em;text-indent:-3.2em;list-style:none}.mw-parser-output .refbegin-100{font-size:100%}
- 诺贝尔化学奖
- 元素列表
- 化学工业
- 化学物质列表
- 化学术语列表
- 化学反应方程式列表
- 元素周期表
- 化学家
- 同位素列表
- 化學基本主題列表
- 化學與物理學的比較
註釋及参考資料
^ Chemistry.(n.d.). Merriam-Webster's Medical Dictionary. Retrieved August 19, 2007.
^ 北京师范大学,华中师范大学,南京师范大学无机化学教研组. 无机化学第四版. 北京: 高等教育出版社. 1981年12月. ISBN 9787040107685 (中文).
^ What is Chemistry?
^ Matter: Atoms from Democritus to Dalton by Anthony Carpi, Ph.D.
^ 5.05.1 沈国威. 译名“化学”的诞生 (PDF). 自然科学史研究. 2000, 19 (1): 55–71. (原始内容 (PDF)存档于2013-07-31). 无效|dead-url=bot: unknown(帮助)
^ 參看《朗文化學詞典》,香港:朗文出版社出版,1997年
^ 有關「化學」一詞的譯名來源亦可參看译名「化学」的诞生[永久失效連結]
^ 註釋:「舍密」一字是音譯自荷蘭語中的"chemie"一字的
^ Hill, J.W.; Petrucci, R.H.; McCreary, T.W.; Perry, S.S.(2005). General Chemistry (4th ed.). Pearson Prentice Hall. p. 37.
^ IUPAC Nomenclature of Organic Chemistry
^ IUPAC Provisional Recommendations for the Nomenclature of Inorganic Chemistry (2004) [1]
^ "Top 50 Chemical Producers". Chemical & Engineering News 83(29): 20–23. July 18, 2005. http://pubs.acs.org/cen/coverstory/83/8329globaltop50.html
参考文獻
从维基百科的姊妹计划 了解更多有关 “化学”的内容 | |
| 维基词典上的字词解释 | |
| 维基共享资源上的多媒体资源 | |
| 维基新闻上的新闻 | |
| 维基语录上的名言 | |
| 维基文库上的原始文献 | |
| 维基教科书上的教科书和手册 | |
| 维基学院上的學習资源 | |
- Atkins, P.W. Galileo's Finger(Oxford University Press)ISBN 978-0-19-860941-4
- Atkins, P.W. Atkins' Molecules(Cambridge University Press)ISBN 978-0-521-82397-5
- Stwertka, A. A Guide to the Elements(Oxford University Press)ISBN 978-0-19-515027-8
- Chang, Raymond. Chemistry 6th ed. Boston: James M. Smith, 1998. ISBN 978-0-07-115221-1
- Atkins, P.W., Overton, T., Rourke, J., Weller, M. and Armstrong, F. Shriver and Atkins inorganic chemistry(4th edition)2006(Oxford University Press)ISBN 978-0-19-926463-6
- Clayden, J., Greeves, N., Warren, S., Wothers, P. Organic Chemistry 2000(Oxford University Press)ISBN 978-0-19-850346-0
- Voet and Voet Biochemistry(Wiley)ISBN 978-0-471-58651-7
- Atkins, P.W. Physical Chemistry(Oxford University Press)ISBN 978-0-19-879285-7
- Atkins, P.W. et al. Molecular Quantum Mechanics (Oxford University Press)
- McWeeny, R. Coulson's Valence(Oxford Science Publications)ISBN 978-0-19-855144-7
- Pauling, L. The Nature of the chemical bond(Cornell University Press)ISBN 978-0-8014-0333-0
- Pauling, L., and Wilson, E. B. Introduction to Quantum Mechanics with Applications to Chemistry(Dover Publications)ISBN 978-0-486-64871-2
- Stephenson, G. Mathematical Methods for Science Students(Longman)ISBN 978-0-582-44416-4
- Smart and Moore Solid State Chemistry: An Introduction(Chapman and Hall)ISBN 978-0-412-40040-7
外部連結
- 英国皇家化学学会
- 美国化学协会
| ||||||
| ||||||||||||||||||||||||||||||
|

Comments
Post a Comment