分子马达
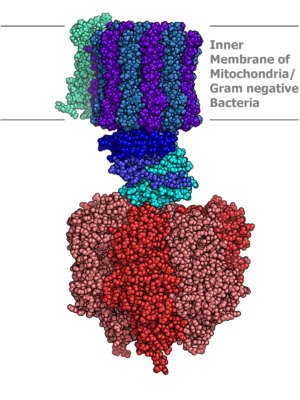
FOF1三磷酸腺苷合酶(ATP synthase / ATPase)分子模型
分子马达(Molecular motor)是分布于细胞内部或细胞表面的一类蛋白质,它负责细胞内的一部分物质或者整个细胞的宏观运动。生物体内的各种组织、器官乃至整个个体的运动最终都归结为分子马达在微观尺度上的运动。分子马达將化学键中的能量耦合转化为动能。而化学键中的能量最终来自细胞膜或线粒体膜内外的电化学梯度。
目录
1 例子
2 实验方法
3 参考文献
4 外部链接
5 参见
例子
一些在生物学中较为重要的分子马达[1]:
细胞骨架马达蛋白:
肌球蛋白主要功能之一是使肌肉收缩。在非肌肉组织中维持细胞的弹性,以及参与细胞质分裂。
驱动蛋白以微管为轨道的动力蛋白,运动的极性由三磷酸腺苷水解酶(ATP水解酶)活性域在蛋白一级结构中的位置决定。
动力蛋白一般是以超分子集成体的形式存在,往微管的负极运动。
聚合马达蛋白:
肌动蛋白聚合作用产生用于推进的力。该过程需要利用三磷酸腺苷(ATP)水解释放的能量。- 微管聚合作用需要利用三磷酸鸟苷(GTP)。
发动蛋白主要功能是从细胞膜中分离网格蛋白芽。该过程需要利用GTP。
转动马达蛋白:
- F0F1三磷酸腺苷合成酶(ATPase)位于细胞膜或线粒体膜上。利用电化学质子的梯度合成ATP[2]。
- 转动马达蛋白令大肠杆菌(E. coli)和其他一些细菌的鞭毛像螺旋桨一般转动,使它们完成游动、翻滚或转向的动作。这种蛋白质由跨膜质子流驱动,运作机制可能与中利用到的Fo马达相似。
核酸马达蛋白:
DNA聚合酶以一条单链DNA为模板合成与之互补的DNA单链[3][4]。
RNA聚合酶(RNAP)以一条单链DNA为模版转录合成与之互补的RNA单链[5]。
解旋酶将双链的核酸分解为在复制和转录中需要利用到的单链。该过程需要利用ATP。
拓扑异构酶降低细胞中DNA的超螺旋数目。该过程需要利用ATP。
RSC和SWI/SNF复合物重塑真核细胞中的染色质。该过程需要利用ATP。
染色体结构维持蛋白被利用于真核细胞中的染色体凝聚[6]。
病毒DNA的包装马达蛋白在病毒的复制周期内将其DNA注入其衣壳中,使该DNA分子被衣壳蛋白紧密包裹起来[7]。
微丝聚合可产生推动力。- 人工合成的动力分子已被一些化学家制出。它们通过改变分子的手性产生扭矩,从而在宏观上产生转向力。
实验方法
- 高清晰度活体显微镜技术
- 广视野显微镜与三维去卷积(decovolution)技术
- 共焦距显微镜(confocal microscopy)技术
- 扫描共焦距激光显微技术(laser-scanning microscopy)
- 转碟共焦距显微镜技术(spinning-disc confocal microscopy)
- 全反射(Total Internal Reflection)与倾斜入射(Oblique illumination)激光显微镜技术
- 共焦距显微镜(confocal microscopy)技术
- 动力分子的主要研究方法还包括分子物理学中的一些技术:
- 荧光共振能转技术(FRET),以及荧光交互波谱分析(FCS)
- 单分子电生理分析(Electrophysiology),用于测量单个离子通道(ion channel)的动力学
- 单分子滑动化验法(single molecule gliding assay),用于测量动力分子的运动速度,弹簧常数,以及processivity.
光鑷,用于测量动力分子的力学性质
参考文献
^ Nelson, P.; M. Radosavljevic, S. Bromberg. Biological physics. Freeman. 2004. 引文使用过时参数coauthors (帮助)
^ Tsunoda SP, Aggeler R, Yoshida M, Capaldi RA. Rotation of the c subunit oligomer in fully functional F1Fo ATP synthase. Proc. Natl. Acad. Sci. U.S.A. January 2001, 98 (3): 898–902. PMC 14681. PMID 11158567. doi:10.1073/pnas.031564198.
^ I. Hubscher, U.; Maga, G.; Spadari, S. Eukaryotic DNA polymerases. Annual Review of Biochemistry. 2002, 71: 133–63 / 133. PMID 12045093. doi:10.1146/annurev.biochem.71.090501.150041.
^ Smith DE, Tans SJ, Smith SB, Grimes S, Anderson DL, Bustamante C. The bacteriophage straight phi29 portal motor can package DNA against a large internal force. Nature. October 2001, 413 (6857): 748–52. PMID 11607035. doi:10.1038/35099581.
^ Dworkin J, Losick R. Does RNA polymerase help drive chromosome segregation in bacteria?. Proc. Natl. Acad. Sci. U.S.A. October 2002, 99 (22): 14089–94. PMC 137841. PMID 12384568. doi:10.1073/pnas.182539899.
^ Peterson C. The SMC family: novel motor proteins for chromosome condensation?. Cell. 1994, 79 (3): 389–92. PMID 7954805. doi:10.1016/0092-8674(94)90247-X.
外部链接
Cymobase - 关于细胞骨架及分子马达蛋白序列资料的数据库
参见
- 分子力学
- 蛋白质动力学
- 马达蛋白
- 细胞骨架

Comments
Post a Comment